| |
|
|
|
|
|
| |
 |
|
神経疾患・精神疾患 |
|
|
| |
|
|
神経疾患・精神疾患とマイコプラズマ感染 |
|
|
| |
|
|
脳炎および髄膜炎とマイコプラズマ感染
マイコプラズマは、急性気管支炎の原因の第1位、肺炎の原因の第3位です。
全身性の血管炎/神経炎であり、喘息・関節炎・腎炎・髄膜炎・脳炎・血管炎・皮膚炎などを引き起こします。
このように、マイコプラズマ感染症は、肺炎のみでなく、全身性のスペクトラム疾患であり、多彩な症状と多様な臨床経過が特徴です。
小児科領域において、肺炎を中心とした呼吸器感染症の原因として重要ですが、時として中枢神経系合併症をひき起こすことがあります。
中枢神経系合併症の頻度 は、2~7%とされています。最も多い神経障害は、 脳炎、髄膜脳炎であり、ついで多発神経炎、小脳炎、脊髄炎、脳血管障害が知られています。感染部位により、多様な症状が診られます。
潜伏期は、だいたい2-3週間ですが、マイコプラズマに接触してから1ヶ月経過したのちにマイコプラズマ肺炎が発症することもあります。潜伏期が比較的長く、症状も、長引いたり、繰り返したりしながら、長期化・慢性化します。
また、潜伏期が比較的長いため、オフィスや学校などで流行が起こると、流行が数ヶ月続くことがあります。
マイコプラズマ感染では、3年から5年で、感染を繰り返します。インフルエンザでは、1年から2年で感染を繰り返すのと同様です。以前、マイコプラズマ肺炎になったからといって、マイコプラズマ感染症にならないとは限りません。
呼吸器症状などが顕著でなくても髄膜炎などのほかの症状から発症することがあるのでこれも注意が必要です。米国で、マイコプラズマ感染によると考えられる脳炎あるいは急性散在性脳脊髄炎(ADEM)など、マイコプラズマ感染による重篤な神経系疾患の多発が考えられ、学校閉鎖により感染の拡大を防いだという報告があります。
マイコプラズマ感染症は、免疫難病の原因としても知られています。リウマチ性疾患や神経系疾患などと区別の難しい、多彩な症状を呈することもあります。
神経難病、ギラン・バレー症候群もその一つです。炎症性脱髄性末梢神経障害、四肢の遠位筋、近位筋の筋力低下などが特徴です。先行感染としては上気道感染が多く、胃腸症状を呈する感染がそれにつづきます。
小児免疫難病、ヘノッホ・シェーンライン紫斑病は、全身性の小血管炎を主徴とし、紫斑、関節炎、糸球体腎炎 (IgA腎症) などの症状を呈します。小児(4~7才)に多発し、秋から冬に多く発症する疾患です。
川崎病も小児の免疫難病です。川崎病は、おもに乳幼児がかかる全身の血管炎症候群の一つです。血管が全身性に炎症を起こすことで、発熱、発疹、冠動脈病変などの様々な症状を惹き起こします。夏と冬に多く地域流行性があることから、感染症が引き金となって起こる可能性が示唆されています。マイコプラズマ感染症でも同様の症状を呈することが報告されています。
これらは、マイコプラズマ感染により発症することがよく知られている免疫難病です。
マイコプラズマは、細胞壁を持たない最小の細菌であり、ウイルスに似た全身性の症状を引き起こす、いわゆる、ウイルス性細菌です。マイコプラズマ感染症は、多様な臨床経過が特徴です。そのため、従来の肺炎やながびく急性気管支炎症状から、診断を進めていく診断システムでは対応できていないのが現状です。
呼吸器症状が顕著でない無菌性髄膜炎が流行してその原因がマイコプラズマであった事例から考えると、スチィーブンス・ジョンソン症候群や川崎病など他の症状から発症した症例においてもマイコプラズマ感染症を念頭に置いた医療が必要になってきます。
マイコプラズマ(Mycoplasma pneumoniae)は、名前の通り肺炎を来す代表的な真正細菌ですが、肺外合併症として脳炎を来すことがあります(2-7%)。血清マイコプラズマ抗体はPA法(主にIgM)≧320倍、CF(主にIgG)≧64倍を陽性とします。抗糖脂質抗体の関与も疑われています。
髄液中のマイコプラズマ抗体が検出されることもありますが、神経症状を呈さないマイコプラズマ感染者でも陽性になることがあり解釈には注意が必要です。
マイコプラズマ感染症は、呼吸器症状とともに中枢神経症状も主要な所見です。中枢神経症状について数多くの所見があります。マイコプラズマ入院患者の7%で、中枢神経症状がみられるという報告があります。よく見られる中枢神経症状は、脳炎、無菌性髄膜炎、多神経炎などです。マイコプラズマ感染症で、1000人に一人の割合で、中枢神経症状がみられるといわれています。
米国疾病予防センターのホームページで、専門家によると通常の肺炎の50人に1人から10人がマイコプラズマ感染と推定しているが、すべてに患者が診断されているわけではないと述べている。また、症状のある患者の3人に一人が肺炎になるのではないかといわれている。現状では、米国全体のマイコプラズマ感染症サーベイランスシステムはないが、米国で毎年200万人が肺炎となり、健康への問題や感染実態は実際より低く見積もられているという。脳炎、腎機能障害、スティーブンスジョンソン症候群、溶血性貧血などの合併症についても述べられている。
関連リンク
- IDWR感染症の話:無菌性
- Tjhie JH, van de Putte EM, Haasnoot K, van den Brule AJ, Vandenbroucke-Grauls CM.
Fatal encephalitis caused by Mycoplasma pneumoniae in a 9-year-old girl.Scand J Infect Dis. 29:424-5. (1997)
- Daxboeck F, Blacky A, Seidl R, Krause R, Assadian O. Diagnosis, treatment, and prognosis of Mycoplasma pneumoniae childhood encephalitis: systematic review of 58 cases. J Child Neurol. 19:865-671. (2004)
- Lin WC, Lee PI, Lu CY, Hsieh YC, Lai HP, Lee CY, Huang LM. Mycoplasma pneumoniae encephalitis in childhood. J Microbiol Immunol Infect. 35:173-178. (2002)
Mycoplasma pneumoniae and central nervous system complications: a review.
http://www.ncbi.nlm.nih.gov/pubmed/16099235
CNS manifestations associated with Mycoplasma pneumoniae infections: summary
of cases at the University of Helsinki and review.
http://www.ncbi.nlm.nih.gov/pubmed/8399938
CD|Mycoplasma pneumoniae Infection Home|Surveillance and Reporting
https://www.cdc.gov/pneumonia/atypical/mycoplasma/surv-reporting.html
|
|
|
脱髄疾患とマイコプラズマ感染
脱髄疾患(demyelinating disease)とは神経疾患の一種で、有髄神経の髄鞘が障害されることで起こる疾患。
有髄神経の周りには髄鞘と呼ばれるものが取り巻いている。これを形成する細胞は、中枢神経では乏突起膠細胞、末梢神経ではシュワン細胞である。この髄鞘があるために有髄神経では跳躍伝導を行うことができるため、これが障害されることで神経伝導速度が遅くなり、多彩な神経症状が引き起こされる。
大きく分けて中枢神経系と末梢神経系の疾患がある。
- 中枢神経系:
- 多発性硬化症、視神経脊髄炎(Devic症候群)、急性散在性脳脊髄炎(ADEM)
- 炎症性広汎性硬化症(Schilder病)、感染性亜急性硬化症全脳炎(SSPE)、感染性進行性多巣性白質脳症(PML)、ビタミンB12欠乏症
- 末梢神経系:
- ギラン・バレー症候群、フィッシャー症候群、慢性炎症性脱髄性多発根神経炎
これらの中にはマイコプラズマ感染症との関連との関連がわかっているものがも多くある。従来の検査法では困難でしたが、原因がマイコプラズマ感染症と診断できれば治療法が見えてきます。 |
|
多発性硬化症(multiple sclerosis; MS)とは中枢性脱髄疾患の一つで、脳、脊髄、視神経などに病変が起こり、多様な神経症状が再発と寛解を繰り返す疾患である。日本では特定疾患に認定されている指定難病です。
中枢性脱髄疾患の中では患者が最も多いです。北米、北欧、オーストラリア南部では人口10万人当たり30〜80人ほどの罹患ですが、アジアやアフリカでは人口10万人当たり4人以下で、人種によって罹患率に大きな差があることが特徴です。
日本での有病率は増加してきており、10万人あたり8 - 9人、人口辺り約12,000人程度であることが2006年神経免疫班会議で報告されています。罹患のピークは30歳頃であり、約80%が50歳までに発症します。また女性に多い。
さまざまな説が唱えられているが未だ原因は不明です。このうち遺伝、自己免疫、ウイルスやマイコプラズマなどの感染の可能性が高いと思われています。再発と寛解を繰り返すという病態からウイルスやマイコプラズマ感染が疑われています。
病巣の周囲にリンパ球やプラズマ細胞が集まっている、免疫グロブリンが沈着、サプレッサーT細胞が減少し、ヘルパーT細胞のTh1タイプが増加、免疫抑制剤が治療に有効、など免疫異常を疑わせる所見が見られます。
日本をはじめとするアジア地域では、視神経と脊髄を病変の主体とする比較的症状の重い視神経脊髄型多発性硬化症が多いとわれています。現在、視神経脊髄型多発性硬化症は、欧米の視神経脊髄炎(Neuromyelitis
optica)と同一病態と考えられています。
主として視神経と脊髄に由来する症候を呈する患者は、従来、視神経脊髄型多発性硬化症(opticospinal MS:OSMS)と呼ばれていましが、その中には視神経脊髄炎(neuromyelitis
optica:NMO)病態を有する患者が含まれています。NMOは、視神経と脊髄を比較的短期間に強く障害する炎症性の病態を背景にした、再発しない疾患として知られていたが、近年、再発性の病態が一般的であることが明らかにされてきています。
自然経過から多発性硬化症は再発寛解を繰り返す再発寛解型MS(RRMS:relapseing-remitting MS)と発症当初から慢性進行性の経過をたどる一次性進行型MS(PPMS:primary
progressive MS)に大別されます。再発寛解型MS(RRMS)の約半数は発症後15~20年の経過で再発がなくても次第に障害が進行するようになり二次性進行型MS(SPMS:secondary
progressive MS)という名称となります。再発は炎症過程を示しており進行は変性過程を示していると考えられています。欧米白人ではRRMSが80~90%でありPPMSが10~20%を占めるが日本人ではPPMSは5%前後です。
劇症型多発性硬化症(MS)は、大脳、脳幹、脊髄などの多彩な症状が2~3週間のうちに出現し昏睡など顕著な意識障害をきたし数週間から数ヶ月のうちに寛解をみることなく死に至る、劇症の経過をとるMSです。剖検例では急性散在性脳脊髄炎と異なり比較的大きな典型的なMSの肉眼的脱髄斑が多数認められます。
MSは寛解と再発を繰り返す中枢神経系の炎症性脱髄を主として軸索変性を伴う疾患です。MSは中枢神経系脱髄疾患のなかで最も多く、炎症、脱髄、グリオーシスを三主徴とし寛解、再燃、進行性の経過をとります。健康な若年成人を主として侵す疾患であり、時に発症数週間から数ヶ月間疲労、脱力感、筋痛、関節痛がみられることもあります。
発症の誘因としてはとして過労、ストレス、ウイルスやマイコプラズマ感染などが上げられています。前駆症状として、頭痛、発熱、感冒様症状、悪心、嘔吐などが10%程度に認められます。また過呼吸や動作時などに急に構音障害や失調症、手足のしびれや痒みなど突発性発作が現れることがあります。
MSの初発症状は脱髄病巣の部位によって多彩です。神経学的所見では無症状であると考えられた部位にも異常が認められることがあります。実際に自覚症状が片側であっても、神経学的所見では両側に異常が認められることもあります。
日本では視力低下が最も多く、上下肢の運動麻痺、四肢頸部体感などのしびれ感がこれにつぐ。全経過中に出現する頻度は、視力低下や視神経萎縮が多い。MSでは中枢神経障害に基づく症候であればどんなものでも出現しうる。MSと診断された後は多くの神経症症候が定期的に生じうる。
MSの25%に初期症状として球後性視神経炎がみられます。視力の低下、視野の異常、中心暗点が特徴的です。
全身型のMSではおよそ半分くらいに視神経炎、脳幹、大脳、脊髄障害の症状や徴候が様々な程度呈してくる。視神経炎が両側に起こり失明に至るような顕著な視力低下を呈する場合にはMSよりも視神経脊髄炎として診断される。
急性脊髄炎(横断性脊髄炎)は、MSの場合、左右非対称に生じ、不完全であることが多い。急性脊髄炎のみがみられその他の脱髄性病変が示唆されたない場合には全身性エリテマトーデスや混合性結合組織病、抗リン脂質抗体症候群による可能性も考慮して診断されます。
多発性硬化症(multiple sclerosis; MS)は中枢神経系の慢性炎症性脱髄疾患であり、時間的・空間的に病変が多発するのが特徴です。通常、詳細な病歴聴取や経時的な神経学的診察により時間的・空間的な病変の多発性を証明し、他の疾患を否定することで診断が確定します。しかしMRIを撮像すると、実際には症状を出した病巣の何倍もの数の炎症性脱髄病巣が中枢神経組織に出現していることが知られています。
急性増悪を繰り返す再発寛解型(RRMS)と発症時から急性増悪がなく1年以上にわたり徐々に病状が進行していく一次進行型(PPMS)は、McDonald基準によりMRI所見や髄液所見を考慮して高い精度で早期診断することが可能といわれています。
現在のところ、MSに特異的なバイオマーカーは知られておらずMSの診断には他疾患の除外が必要です。神経症状の増悪を認めなくとも定期的なMRI撮影が必要である。画像上病変の増加が認められることがあります。注意するべきこととしてMRIで異常が認められなくともMSの再発は否定出来ないため、また、髄液検査でも異常が見られないこともあり、症状から再発が強く疑われたときは治療をすることが必要となります。
急性脱髄性炎症に伴う軸索の切断は早い時期から生じていることが病理学的に証明されています。中枢神経の可塑性や再髄鞘化により再発は病初期は回復しやすい。しかし、次第に軸索障害が蓄積することにより再発後に後遺症を残すようになります。再発頻度は発症後数年が最も高率であり経過が長くなるにつれ年間再発率は自然に減少します。
関連リンク
難病情報センター | 多発性硬化症/視神経脊髄炎
http://www.nanbyou.or.jp/entry/3806
|
急性散在性脳脊髄炎(acute disseminated encephalomyelitis;ADEM)と多発性硬化症
急性散在性脳脊髄炎(ADEM)とは、ウイルスやマイコプラズマ感染後やワクチン接種後に生じる脳脊髄炎です。
急性散在性脳脊髄炎(ADEM)は炎症性脱髄疾患で、有髄神経線維のミエリンがなくなる病気です。多くの場合、白質の静脈周囲、もしくは灰白質の一部に多発性の炎症性脱髄を認めます。
原因別に1)感染後ADEM、2)ワクチン接種後ADEM、3)特発性ADEMがあります。感染後ADEMは、一般的には気道、消化管感染症などの後に起こりますが、起炎病原体を同定されないことが多い。
感染後ADEMは小児に発症することが多く、特発性ADEMは若年成人に多い傾向があるといわれています。わが国における有病率は、人口10万人あたり2.5人くらいとされています。
症状は、感染後あるいはワクチン接種後、数日~4週後(多くは1~2週後)に急性に発症し、基本的には単相性の経過をとります。つまり、再燃したり、軽快・増悪を繰り返すことはないといわれています。病変部位により症状は多彩で、初期症状として髄膜刺激症状(頭痛、悪心、嘔吐、項部硬直、発熱、Kernig徴候など)を認めやすく、通常の脳炎型では髄膜刺激症状以外に、意識障害、痙攣、片麻痺、失語、脳神経麻痺、小脳症状(眼振、小脳失調など)などがみられます。
病初期は他疾患との鑑別が非常に困難であるため、病状の経過から総合的に診断するしかありません。基本的に先行する感染症状およびワクチン接種の有無が診断の助けとなるため、特にくわしい病歴を聴取することが非常に重要です。
血液所見では末梢血の白血球増加、赤沈亢進、CRP陽性などを認めます。髄液所見では髄液圧の軽度上昇、軽度~中等度のリンパ球優位の細胞数上昇、正常ないし軽度の蛋白上昇、糖は正常範囲です。IgGも上昇し
、髄液オリゴクローナルバンド陽性となることもあります。髄液塗抹検査、培養検査やPCRなどで、病原体は検出できない。(PCRによる検出は検体の安定性や採取時期や場所の問題があり、検出できないからといってマイコプラズマ感染を否定はできない。)
画像診断では、CTにて病変部位で低吸収域を示します。MRIではT2強調画像で高信号域を示します。治療回復後の病変の大きさと数は、減少するか完全に消失します。脊髄MRIでは脊髄病変部の腫大、T2強調画像で高信号域、Gdによる造影効果陽性などを認めます。脳波所見は、4~6Hzの高振幅徐波を、通常は全般性対称性に認めます。時に片側性あるいは巣状です。
鑑別診断として多発性硬化症(MS)、感染性脳炎(マイコプラズマ脳炎、急性ウイルス性脳脊髄炎、日本脳炎、ライム病等)、髄膜炎(ウイルスやマイコプラズマなどによるもの、結核性のもの)、Reye症候群、SLE、高リン脂質抗体症候群(APS:antiphospholipid syndrome)、神経べーチェット病などが挙げられます。
とくに、多発性硬化症と急性ウイルス性脳脊髄炎との鑑別が重要です。最小の細菌であるマイコプラズマも、ウイルス性の脳脊髄炎症状の原因になります。急性ウイルス性脳脊髄炎の中でも単純ヘルペス脳炎は、重篤ではありますが治療可能な疾患であり、早期に発見して抗ウイルス薬を投与する必要があります。MSとの鑑別は困難なことが少なくありません。
MSではADEMに比較して全身の炎症所見に乏しく、症状の寛解や再発(時間的多発性)をみることで鑑別します。MSでは経時的MRIで病変の増加を認めますが、ADEMでは増加しないという点で鑑別に有効ですが、初回発作時はCT、MRI所見も鑑別には役に立たず限界があります。
ADEMは多発性硬化症(multiple sclerosis; MS)の類縁疾患で、重要な鑑別疾患です。ADEMとの共通点はどちらも脱髄疾患であることですが、ADEMではMSの初期と同じように回復するといわれています。MSの経過は、再発/緩解の経過をたどる場合もあれば、進行性の経過をたどる場合もある。良性の経過をたどるものから、急速に進行して生活そのものが困難になる深刻な経過をたどる場合もあります。実際は、初期は区別が困難。治療として、憎悪時にはADEMと同様まずステロイドパルス療法を試みる。その他は対症療法である。いろいろな治療法を試みられているが説得力に欠けるものが多い。(原因が特定できれば、原因根治的な治療が可能になってきます。)
|
ADEM とマイコプラズマ感染症
ADEMは、特に、、多発性硬化症と急性ウイルス性脳脊髄炎との鑑別が重要です。最小の細菌であるマイコプラズマも、ウイルス性の脳脊髄炎症状の原因になります。
マイコプラズマは、結膜(結膜炎)、気管支(気管支炎)、肺炎などで、簡単にウイルスのように血液中に侵入し、下記のように、微小血管周囲や神経組織などに侵入して増殖することがわかっています。免疫機能が低い場合だけでなく、健常人でも子供や成人でも感染したときのマイコプラズマの量や免疫状態によっては、重症化、慢性化します。慢性化していく場合、抗原測定法をはじめ従来の方法では、診断がつきません。
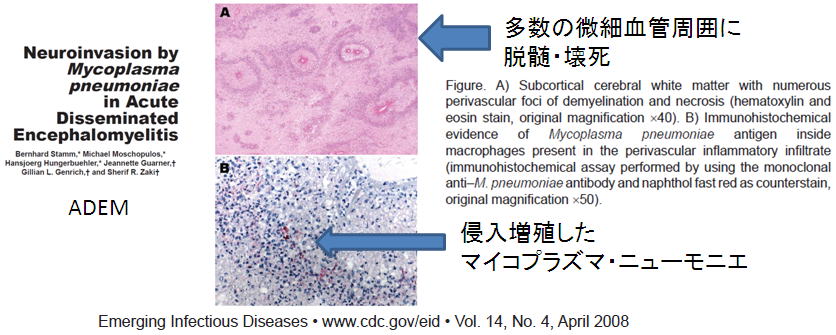
Neuroinvasion by Mycoplasma pneumoniae in acute disseminated encephalomyelitis.
http://www.ncbi.nlm.nih.gov/pubmed/18394283
Direct invasion of the central nervous system by Mycoplasma pneumoniae: a report of two cases.
http://www.ncbi.nlm.nih.gov/pubmed/3100660
Acute disseminated encephalomyelitis in children and adolescents: a single center experience.
http://www.ncbi.nlm.nih.gov/pubmed/23849604
Three cases of central nervous system complications associated with Mycoplasma pneumoniae.
http://www.ncbi.nlm.nih.gov/pubmed/15301835
Mycoplasma pneumoniae: nervous system complications in childhood and review of the literature.
http://www.ncbi.nlm.nih.gov/pubmed/18506483
Neurological complications associated with Mycoplasma pneumoniae infection. A case report.
http://www.ncbi.nlm.nih.gov/pubmed/11028161
Mycoplasma pneumoniae and central nervous system complications: a review.
http://www.ncbi.nlm.nih.gov/pubmed/16099235
CNS manifestations associated with Mycoplasma pneumoniae infections: summary
of cases at the University of Helsinki and review.
http://www.ncbi.nlm.nih.gov/pubmed/8399938
|
視神経脊髄炎(Neuromyelitis optica)と多発性硬化症
視神経脊髄炎(neuromyelitis optica)は、重度の視神経炎と横断性脊髄炎を特徴とする疾患です。Devic病とも呼ばれています。多発性硬化症(MS)、急性散在性脳脊髄炎(ADEM)との異同が長らく議論されてきました。
視神経脊髄炎(neuromyelitis optica:NMO)は、視神経と脊髄を比較的短期間に強く障害する炎症性の病態を背景にした、再発しない疾患として知られていたが、近年、再発性の病態が一般的であることが明らかにされてきています。
主として視神経と脊髄に由来する症候を呈する患者は、従来、視神経脊髄型多発性硬化症(opticospinal MS:OSMS)と呼ばれていましが、その中には視神経脊髄炎(neuromyelitis optica:NMO)病態を有する患者が含まれています。
現在、視神経脊髄型多発性硬化症は、欧米の視神経脊髄炎(Neuromyelitis optica)と同一病態と考えられています。日本をはじめとするアジア地域では、視神経と脊髄を病変の主体とする比較的症状の重い視神経脊髄型多発性硬化症が多いとわれています。
現状では、診断基準では全身性エリテマトーデス、シェーグレン症候群など膠原病や膠原病類縁疾患の徴候があった場合はその病変はNMOではなく、膠原病や膠原病類縁疾患の中枢神経症状と考えられています。シェーグレン症候群、全身性エリテマトーデス、橋本病など自己免疫病を合併する例が多ことが知られています。
初発症状では視力障害が多い。MSでは片側性の視力障害が多いのに対してNMOでは両側性の視力障害を呈することが多い。
|
視神経脊髄炎(Neuromyelitis optica)とマイコプラズマ感染
視神経脊髄炎(neuromyelitis optica)は、重度の視神経炎と横断性脊髄炎を特徴とする疾患です。Devic病とも呼ばれています。多発性硬化症(MS)、急性散在性脳脊髄炎(ADEM)との異同が長らく議論されてきました。
視神経脊髄炎(neuromyelitis optica:NMO)は、視神経と脊髄を比較的短期間に強く障害する炎症性の病態を背景にした、再発しない疾患として知られていたが、近年、再発性の病態が一般的であることが明らかにされてきています。
Mycoplasma pneumonia as a cause of neuromyelitis optica?
http://www.ncbi.nlm.nih.gov/pubmed/18563469
Guillain-Barré syndrome (GBS) with bilateral optic neuritis and central white matter disease.
http://www.ncbi.nlm.nih.gov/pubmed/8469352
Bilateral optic neuritis following Mycoplasma pneumoniae infection.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4313507/
Bilateral optic neuritis and Guillain-Barré syndrome following an acute Mycoplasma pneumoniae infection.
http://www.ncbi.nlm.nih.gov/pubmed/15311361
Post-infectious central and peripheral nervous system diseases complicating Mycoplasma pneumoniae infection. Report of three cases and review of the literature.
http://www.ncbi.nlm.nih.gov/pubmed/11784383 |
慢性炎症性脱髄性多発神経炎(chronic inflammatory demyelinating polyneuropathy, CIDP)
慢性炎症性脱髄性多発神経炎(chronic inflammatory demyelinating polyneuropathy, CIDP)は、2ヶ月以上にわたる緩徐進行性あるいは階段性、再発性の経過を示す末梢神経疾患です。通常は四肢対称性、びまん性の(遠位筋と近位筋の両者が障害される)筋力低下と感覚障害を主徴とする。
病因は末梢神経を構成する髄鞘(ミエリン)構成成分に対する免疫寛容の破綻であり、なんらかの自己免疫機序が背景にあると推測されるものの、詳細は明らかではないです。
臨床経過は亜急性または慢性に進行する型(緩徐進行型)、再発と寛解を繰り返す型(再発寛解型)、単回の発症で以後再発のない単相型に大別されます。
国内外における疫学報告には開きがあり、有病率は10万人あたり0.4〜8.9人。
末梢神経を構成する髄鞘(ミエリン)成分に対する障害により発症すると考えられているが、詳細は不明。中枢神経における脱髄をきたす多発性硬化症の合併がごく一部にみられ、多発性硬化症との鑑別が難しいことがあります。
Chronic inflammatory demyelinating polyneuropathy after Mycoplasma pneumoniae infection.
http://www.ncbi.nlm.nih.gov/pubmed/17594309
Severe childhood Guillain-Barré syndrome associated with Mycoplasma pneumoniae infection: a case series.
http://www.ncbi.nlm.nih.gov/pubmed/26115201 |
ギラン・バレー症候群(GBS)とマイコプラズマ感染
ギラン・バレー症候群(GBS)は、急性の運動麻痺をきたす末梢神経障害であり、多くの場合(約7割)呼吸器あるいは消化器感染の後に発症します。
年間の発病率は10万人当たり1~2人程度。
特に60%以上の例で何らかの先行感染が認められる。因果関係がはっきりしているのはウイルスやマイコプラズマなど。マイコプラズマは2週間前程度に上気道炎を先行感染として起こすことが多い。
ワクチンの接種後の発症例も認められている。ワクチンの場合は3週間以上前のことが多い。GBSを疑った場合は、1週間前に下痢をしなかったか、2週間前に咽頭痛や咳、鼻水といった風邪の症状はなかったのか、1か月以内にワクチンの接種をしなかったのかと調査していく必要がある。
四肢の筋力低下を主徴とするが、異常感覚を含めた感覚障害を伴うことも多い。顔面神経麻痺、眼球運動麻痺や嚥下・構音障害などの脳神経障害を伴うこともある。症状の極期には呼吸筋麻痺や自律神経障害を呈する例もある。
腱反射は低下ないし消失します。また、マイコプラズマ肺炎後のGBSでは抗galactocerebroside抗体が上昇するが、Mycoplasma pneumoniaeの菌体にはgalactocerebroside様の糖鎖構造が存在することが報告されています。
Mycoplasma pneumoniae triggering the Guillain-Barré syndrome: A case-control
study.
http://www.ncbi.nlm.nih.gov/pubmed/27490360
Severe childhood Guillain-Barré syndrome associated with Mycoplasma pneumoniae infection: a case series.
http://www.ncbi.nlm.nih.gov/pubmed/26115201
Mycoplasma pneumoniae infection with neurologic complications.
http://www.ncbi.nlm.nih.gov/pubmed/25793076
Cross-reactive anti-galactocerebroside antibodies and Mycoplasma pneumoniae infections in Guillain-Barré syndrome.
http://www.ncbi.nlm.nih.gov/pubmed/12225900
Acute motor axonal neuropathy after Mycoplasma infection: Evidence of molecular mimicry.
http://www.ncbi.nlm.nih.gov/pubmed/15037698 |
筋萎縮性側索硬化症 (amyotrophic lateral sclerosis、ALS)とマイコプラズマ感染
筋萎縮性側索硬化症 (amyotrophic lateral sclerosis、ALS)は、重篤な筋肉の萎縮と筋力低下をきたす神経変性疾患で、運動ニューロン病の一種。極めて進行が速く、半数ほどが発症後3年から5年で呼吸筋麻痺により死亡する(人工呼吸器の装着による延命は可能)。
治癒のための有効な治療法は確立されていません。
日本国内では1974年に特定疾患に認定された指定難病。公費負担の対象疾患です。
Endresen GK. Mycoplasma blood infection in chronic fatigue and fibromyalgia
syndromes. Rheumatol Int. 23:211-215 (2003)
Horner RD, Kamins KG, Feussner JR, Grambow SC, Hoff-Lindquist J, Harati Y, Mitsumoto H, Pascuzzi R, Spencer PS, Tim R, Howard D, Smith TC, Ryan MA, Coffman CJ, Kasarskis EJ. Occurrence of amyotrophic lateral sclerosis among Gulf War veterans.Neurology. 61:742-749. (2003)
Nicolson GL, Nasralla MY, Haier J, Pomfret J. High frequency of systemic mycoplasmal infections in Gulf War veterans and civilians with Amyotrophic Lateral Sclerosis (ALS). J Clin Neurosci. 9:525-529. (2002) |
| |
|
|
|
|
|

![]()

